医薬品残留溶媒分析GCデータ集
医薬品残留溶媒分析GCデータ集
米国薬局方(USP),欧州薬局方(EP)に準拠したヘッドスペースGCによる医薬品残留溶媒分析用にデータ集「ヘッドスペースGC[HS-20+GC-2010 Plus]による医薬品残留溶媒分析データ集」をご用意しました。分析例やLabSolutions(GC)でご利用いただけるメソッドファイルを収載しています。また,米国薬局方(USP),欧州薬局方(EP)準拠の分析法に関する実務者向け解説書もご用意しました。
※本ページでご紹介しているデータ集および解説書をご覧いただくには, My SHIMADZUへの会員登録が必要です。
医薬品残留溶媒分析GCデータ集
島津ガスクロマトグラフィー ヘッドスペースGC[HS-20+GC-2010 Plus]による医薬品残留溶媒分析データ集
米国薬局方(USP),欧州薬局方(EP)準拠
| <内容> ・水に可溶な検体Procedure A,B標準試料分析例 ・水に不溶な検体Procedure A,B標準試料分析例(DMF溶媒-USP試料調製法) ・LabSolutions(GC)用メソッドファイル |
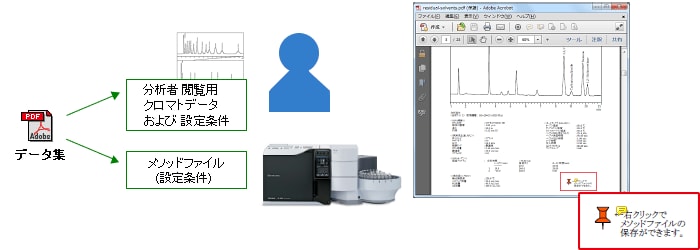
医薬品残留溶媒分析GCデータ集には,分析者が閲覧するクロマトデータ/設定条件,LabSolutions(GC) (Ver.5.45 以降)用のメソッドファイルも含まれています。 PDF内の貼り付けマークのあるところで,右クリックして埋め込まれたメソッドファイルを抜き出してご使用ください。
[ご注意]GCsolutionでは使用できません。
ヘッドスペースGCによる医薬品残留溶媒分析に関する解説書
-米国薬局方(USP),欧州薬局方(EP)準拠の分析法に関する実務者向け解説-
| <内容> 1.概論 2.使用機器について 3.カラムについて 4.試料調製について 5.再現性について 6.ブランク確認について |

医薬品中残留溶媒分析システム
- 医薬品中残留溶媒の分析は,最終製剤,原薬,医薬品添加物などの検体を適当な溶媒に溶解させ,バイアル中に封入し一定時間加熱し,バイアル中の気相部分の揮発成分を分析するヘッドスペース法が主流となっています。
- 医薬品中残留溶媒の分析では,スプリット比の設定が容易であり検出器ガスを含めたフルデジタルを流量制御を行うことのできるキャピラリガスクロマトグラフNexis GC-2030と高い再現性と低いキャリーオーバーによって,いつでも正確な定量ができるヘッドスペースサンプラHS-20の組合せが最適です。
- FIDは,世界最高感度1.5 pgC/secであり,微量溶媒の検出を逃しません。また,ワークステーションLabSolutions(GC)と組み合わせてご使用いただくことにより,ヘッドスペースの分析条件も同一メソッドとして管理,保存が可能です。


