Nexis™ GC-2030+HS-20 による医薬品残留溶媒分析
医薬品残留溶媒の試験法は、第十七改正日本薬局方やUSP(米国薬局方)General Chapters<467> Residual Solvents に規定されており、主にヘッドスペースGC 法が用いられます。医薬品中の残留溶媒はヒトの健康に及ぼし得るリスクに基づいてクラス1 からクラス3 に分類され厳密に管理されていますが、第十七改正日本薬局方第二追補において新たにメチルイソブチルケトン(MiBK)が追加されました。第十七改正日本薬局方第二追補で追加されたMiBK の分析結果を紹介します。またこの成分はUSP においてはクラス2A に分類されており、クラス2A のクロマトグラムと比較して紹介します。
分析条件
ガスクロマトグラフNexis GC-2030 と島津ヘッドスペースガスサンプラHS-20 を接続し、第十七改正日本薬局方第二追補に記載されたクラス2A およびMiBK の標準溶液を測定しました。標準溶液は水溶性試料を調製し、それぞれカラムの種類、カラム温度、スプリット比の異なる操作法A および操作法B で測定しました。水溶性試料の分析条件を表1示します。
水溶性試料 クラス2A およびMiBK 標準溶液分析
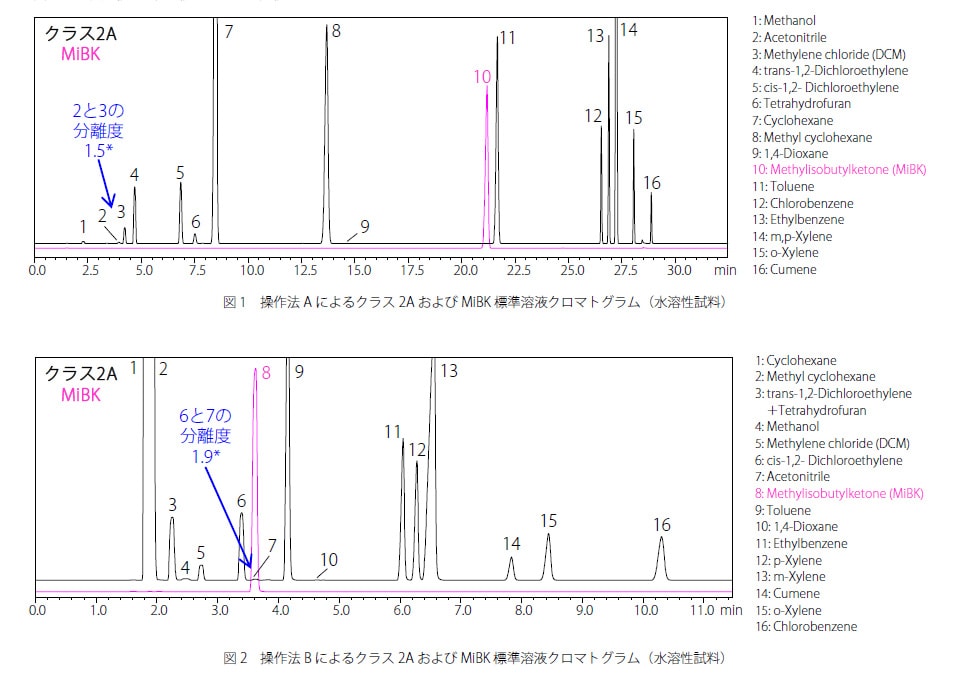
操作法A の分析結果を図1 に、操作法B の分析結果を図2 に示します。(クラス2A:黒、MiBK:ピンク)
*図中に記す分離度は参考値であり、保証値ではありません。
GC 分析条件(操作法A・操作法B)
| Model | Nexis GC-2030 |
| Detector | 水素炎イオン化検出器 FID-2030 |
| Column | A) SH-Rxi™-624 Sil MS (0.32 mm I.D.×30 m, d.f.= 1.8 μm) B) SH-Stabiliwax (0.32 mm I.D.×30 m, d.f.= 0.25 μm) |
| Column temperature | A) 40 ℃ (20 min) ‒ 10 ℃/min ‒ 240 ℃ (20 min) Total 60 min B) 50 ℃ (20 min) ‒ 6 ℃/min ‒ 165 ℃ (20 min) Total 59.17min |
| Injection Mode | A) Split 1:5 B) Split 1:10 |
| Carrier Gas Controller | 線速度 (He) 35 cm/sec |
| Detector Temperature | 250 ℃ |
| Detector Gas | H2 32 mL/min, Air 200 mL/min |
| Make up | 24 mL/min (He) |
| Injection Volume | 1 mL |

医薬品中残留溶媒分析システム
- 医薬品中残留溶媒の分析は,最終製剤,原薬,医薬品添加物などの検体を適当な溶媒に溶解させ,バイアル中に封入し一定時間加熱し,バイアル中の気相部分の揮発成分を分析するヘッドスペース法が主流となっています。
- 医薬品中残留溶媒の分析では,スプリット比の設定が容易であり検出器ガスを含めたフルデジタルを流量制御を行うことのできるキャピラリガスクロマトグラフNexis GC-2030と高い再現性と低いキャリーオーバーによって,いつでも正確な定量ができるヘッドスペースサンプラHS-20の組合せが最適です。
- FIDは,世界最高感度1.5 pgC/secであり,微量溶媒の検出を逃しません。また,ワークステーションLabSolutions(GC)と組み合わせてご使用いただくことにより,ヘッドスペースの分析条件も同一メソッドとして管理,保存が可能です。


