4.2. GC-MSによる定性分析
4.2.1. 定性分析とスキャンモード
長所
■マススペクトルから定性情報が得られる
■目的成分以外の情報が得られる
短所
■SIMモードに比べ,感度が劣る
分析の流れは,定性分析から入るのが一般的です。試料に含まれる成分を知るという以外に,定量分析のスタートポイントとしての定性分析も重要です。
(1)定性分析でよく使用される分析モードはスキャンモードです。スキャンモードではマススペクトルが得られます。
(2)スキャンモードで得られるマススペクトルに対してライブラリ検索を行うことで,化合物同定を行います。化合物の同定にはマススペクトル以外に,保持時間情報も利用できます。
(3)スキャンで得られるマスクロマトグラムを用いて定量を行うこともできます。
スキャンモードで定量作業を行うことも可能ですが,後述のSIMモードに比べ感度が劣ちるという欠点があります。しかし,マススペクトルが得られているので,ターゲット化合物のピークであるかの確認をすぐに行えるメリットもあります。
4.2.2. スキャンモードで得られるデータ
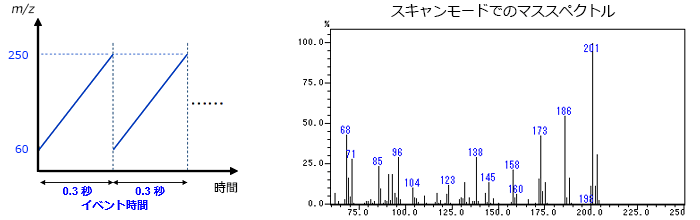
1. 一定時間(例えば0.3秒)毎にマススペクトルを連続採取
2. 全てのデータをPCに格納
スキャンモードでは,分析メソッドで設定されたm/zの範囲を走査して,各m/zのイオン強度を調べます。クロマトグラム上を繰り返し走査し,データをサンプリングします。各サンプリング点において,横軸にm/zを,縦軸に強度(イオンの存在量)をプロットしたグラフがマススペクトルです。1つの分析データは,多数のマススペクトルの集合体です。スキャン速度が速いほど,細かい点間隔でスキャンクロマトグラムを作っていきます。
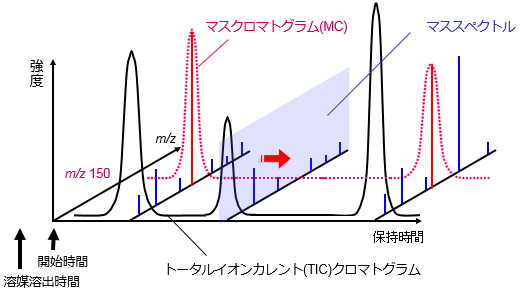
スキャン分析では,様々なクロマトグラムを描かせることが可能です。
(1) TIC(トータルイオンカレント)クロマトグラム:スペクトルの開始m/zから終了m/zまでの全ての強度を合算して表示したクロマトグラムです。スペクトルの測定範囲が十分広ければ,全溶出のクロマトグラムを表しているのでGCのクロマトグラムに似ていると言えます。
(2) マスクロマトグラム(MC):特定のm/zだけを取り出して表示したクロマトグラムです。
4.2.3. ライブラリ検索(シミラリティ検索)
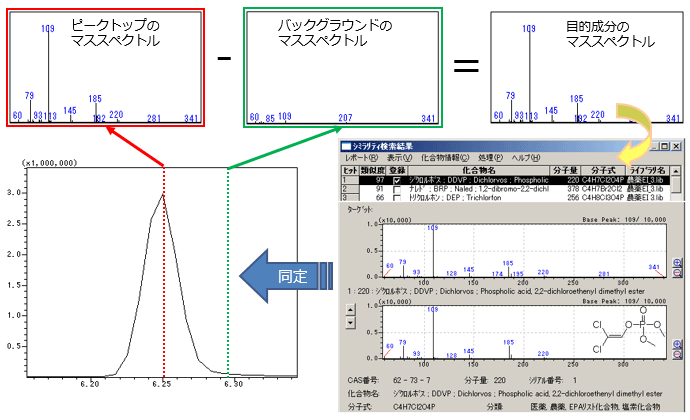
クロマトグラムのピーク成分が何かを決める作業が化合物同定です。この作業で力を発揮するのが,マススペクトルです。
同定作業では,マススペクトルライブラリがよく利用され,測定マススペクトルとライブラリのスペクトルをコンピュータが比較し,その類似度を数値化し,似ている順に並べてユーザに提示してくれます。これをシミラリティ検索や類似度検索,ライブラリ検索などと呼んでいます。
1つのクロマトピークが単成分から構成されているのが理想ですが,バックグラウンド信号が重なってくることもよくあります。この場合,ピークトップのマススペクトル(またはピーク全体の平均スペクトル)から,バックグラウンド領域のマススペクトルを引き算する操作を行うこともあります。この操作をバックグラウンド減算と呼びます。
4.2.4. シミラリティ検索結果
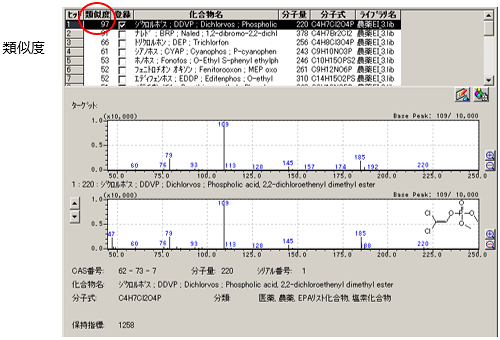
シミラリティ検索の結果は,化合物名と合わせて類似度が表示されます。一般的に類似度が大きいほど,ターゲットマススペクトルと登録されている化合物のスペクトルが類似していることを表します。
理想的には,マススペクトルは化合物ごとに異なりますが,実際は,構造の似た化合物や異性体ではマススペクトルが類似しています。この場合,類似度が近い候補が複数表示され,マススペクトルのみでは同定が難しくなります。この場合,標準試料を用いて保持指標を確認することで,候補を絞り込めます。これを系統的に行うのが,保持指標を用いたシミラリティ検索です。マススペクトルライブラリには,スペクトル以外に,化合物の保持指標値が登録されているものがあり,保持時間の観点からフィルタリングを行い,候補の絞り込みを助けてくれます。
シミラリティ検索結果は,ソフトウェアによる候補化合物の提示です。正しい同定のためには,ユーザ自身による試料の状況や分析の状況からの判断が必要です。
4.2.5. 重なったピークの化合物同定
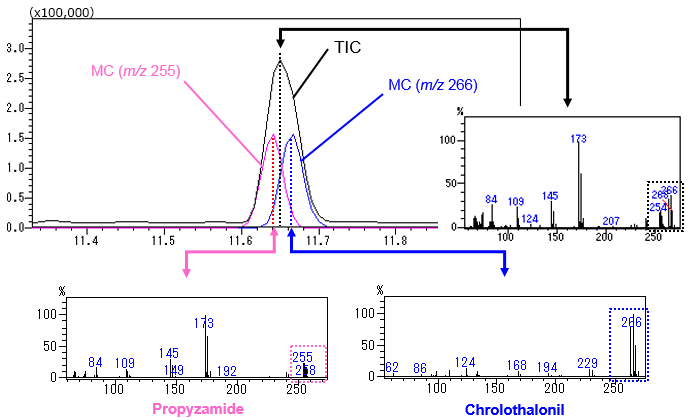
TICでは1つに見えるピークが,実は二つの成分が重なっていることがあります。ピークの前の方と後ろの方でマススペクトルが異なっている場合,2つの成分が重なっている可能性が高くなります。例えば,前の方のマススペクトルで特異的に現れているm/z 255と後ろのほうで特異的に現れているm/z 266でマスクロマトグラムを描かせると,それぞれのピークの頂点は,ずれています。つまり,TICでは1つのクロマトピークに見えていますが,これは,二つの成分が重なってできたものであることがわかります。
さらに,重なったピークの場合,ピークの前の方と後ろの方で別々にライブラリサーチをかけることで,個別に化合物同定できる場合もあります。
4.2.6. マスクロマトグラムによる目的成分のピークの確認
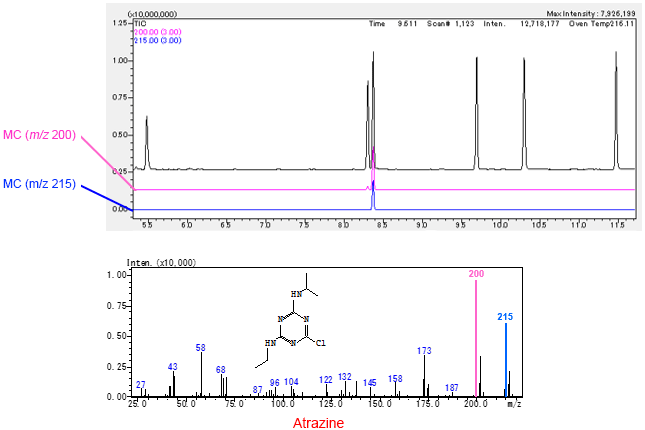
クロマトグラムにピークが非常にたくさんある場合,目的の成分のピークを探すのは,大変な作業です。1つ1つライブラリサーチをするにも時間がかかります。こんな時,マスクロマトグラムを利用して絞り込むことができます。
例えば,Atrazineのピークを探すことを目的として,この化合物のマススペクトルをライブラリで調べてみると,m/z 200とm/z 215に強いマススペクトル成分があります。この2つのクロマトグラムを描かせると,共通して現れているピークは1本だけになり,このピークがAtrazineのピークとわかります。
念のため,このピークに対してシミラリティリサーチを行い,思った通りの結果が得られれば,目的とする成分のピークであることの確証が得られます。


