
LC分析の留意点

金澤 秀子 先生
慶應義塾大学 薬学部 教授 (ご所属・役職は2016年1月発行時)
■「LCtalk」誌の読者は,何らかの形でLCと関わっていらっしゃる方だと思います。もし,その中で『温度応答性クロマトグラフィー』という言葉を知っている方が少しでもいらっしゃれば幸いです。
■私が『温度応答性クロマトグラフィー』という概念を提唱して20年になりました1-3)。 一般にHPLCの専門家といえば,試料を見て,カラムと移動相の選択が瞬時に浮かぶような方というイメージですが,『温度応答性クロマトグラフィー』で は,そのような知識を必要とせず,温度すなわちボタン一つで自由に保持時間をコントロールできるという全く新しい概念のクロマトグラフィーです。
■当時,共同研究者でもある東京女子医大の岡野光夫教授が,温度応答性培養皿を開発しており 温度によって培養皿の表面の性質を変化させて,酵素を使わずに細胞をはがすことができるという研究をされておりました。その独創的な発想に惹かれて,クロ マトグラフィーの充塡剤にも応用しようというのが,この研究の始まりです。これまでのHPLCのように移動相の組成を変化させて分離選択性の制御を行う方 法と異なり,温度応答性高分子を修飾した固定相表面の性質が温度によって変化することを利用して分離選択性の制御を行うというものです(図1)。したがっ て移動相は最も単純な純水を用いて医薬品の分離を行うことができました。
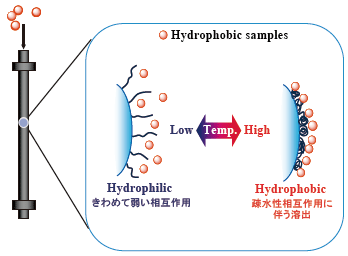 図1. 温度応答性クロマトグラフィー概念図
図1. 温度応答性クロマトグラフィー概念図■私自身は,画期的な方法が発明できたと考えておりましたが,当初は専門家の方たちには,な かなか受け入れてもらうことができませんでした。実際,クロマトグラフィーの移動相に水のみを使うという発想も私どもが初めてであったと思います。現在で は,水100 %の移動相を使用可能なカラムはたくさん出ておりますが,水を使うところは同じですが,温度によって充塡剤の表面の性質を変化させ自由に保持のコントロー ルが可能であるというところが,それらのカラムと『温度応答性クロマトグラフィー』との大きな違いです。
■その後,島津製作所のProminence がPittcon に出展される際に高性能のカラムオーブンであるということで共同研究することになり,私どもの温度応答性カラムを用いて温度グラジエントを行いました。市 販のカラムオーブンを使用し,イソクラティックな条件(単一水移動相)で有機溶媒を用いた時と同様な効果が得られることを証明することができました(図 2)。
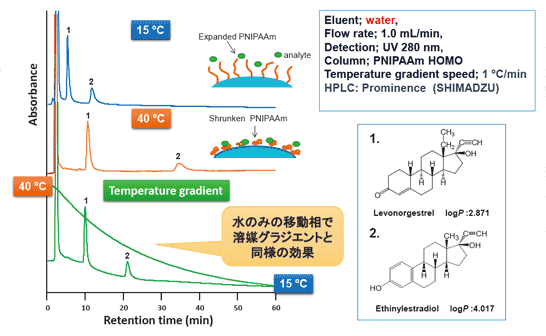 図2. 温度グラジエントによる水移動相を用いたステロイド医薬品の分離
図2. 温度グラジエントによる水移動相を用いたステロイド医薬品の分離■私がHPLCと出会ったのは,大学院生の時でした。当時は,HPLC といってもご存じない方も多く,HPLC(高速液体クロマトグラフィー)と必ず注釈をいれなくてはいけない時代でした。検出器もフォトダイオードアレイが 出始めてきて,3次元のデータ処理のソフトなどを東大の研究者が開発している頃でした。今やHPLCは大学のどこの研究室にもあり,学生実習でも使用する ような汎用機器になっています。私自身は,大学院の博士課程でポアサイズ50 nmのガラスODS充塡剤を使った「超高速HPLC」という研究を行っておりました。「超高速HPLC」という言葉は,今では普通に使っていますが,当時 は現在のシステムとは少し異なりますが,耳新しい言葉でした。驚くべきことにHPLCの装置や充塡剤が大きく進歩した現在でも当時の分離に追いついていな い物質も実際にあります。
■逆相クロマトグラフィーは,医薬品について学ぶ薬学部において大変有用な分離システムで す。私はよく学生に「逆相カラムは皆さんの身体に似ている」と例えています。一般に逆相カラムから早く溶出する薬物は,水溶性であり身体からも速やかに排 泄されますが,カラムに長く保持されるような薬物は脂溶性が高く,排泄されずに身体にとどまるという具合です。つまりHPLC で分析することで,薬の体内での動きがある程度推測できるということになります。低学年で薬の性質を学ぶのに大変わかりやすいと思います。
■温度応答性クロマトグラフィーに使用している機能性高分子Poly(N-isopropylacrylamide) (PNIPAAm)は, 下限臨界溶解温度(lower critical solutiontemperature, LCST)を有し,LCST以下ではポリマー鎖が伸展し水和構造をとりますが,LCST以上ではポリマー鎖が収縮し脱水和するというように温度によって親 水性と疎水性が変化します。生体高分子と同様にコイル-グロビュール転移をします。このような性質をもった機能性高分子は,Biomimeticな材料と して大変興味深い研究対象です。
■例えば我々の身体の薬物受容体における薬物の認識には,複数の分子間相互作用すなわち, ファーマコフォアpharmacophore(疎水性相互作用,水素結合,静電的相互作用,π - π相互作用など)が重要であると考えられています。新規医薬品をデザインする際にも用いられる概念です。クロマトグラフィー分離にもこの概念を取り入れた いと考え,複数の相互作用を高分子設計により構築し,それらを温度などの信号によって外部から制御できるようなカラムを作製しています。現在で は,PNIPAAmにアミノ酸誘導体を共重合した高分子を用いて分子認識能を向上させた充塡剤を開発し4),究極的には生体が分子を見分けるように分子認識ができるクロマトグラフィーの構築を目指しています。
■PNIPAAmなどのBiomimeticな刺激応答性高分子は,細胞との相互作用も大変 興味深く,クロマトグラフィー以外の分野についても機能性高分子を用いた研究を進めています。例えば細胞内外の微小な物理化学的変化が追跡可能な生体可視 化のための環境応答型機能性蛍光プローブを開発しています5)。また標的部位において物理化学的刺激に応答した薬物放出制御が可能となる温度応答性ナノキャリアによるドラッグデリバリーシステム(DDS)も構築しています6)。
参考文献