
LC分析の留意点

越後 信哉 先生
京都大学大学院工学研究科 都市環境工学専攻 都市衛生工学研究室 准教授 (ご所属・役職は2013年7月発行時)
■日本を始め多くの国では,浄水処理において塩素消毒を行い,水中の微生物を不活化して水系感染症のリスクを低減し我々の健康を守ってきた。しかし,最近は水道水の快適性に関する不満から水道水離れが進んでいる。不満の原因の一つが塩素消毒によって発生する臭気,カルキ臭であるとされる。
■カルキ臭の原因は,水道原水中のアンモニウムイオンやアミノ酸と,消毒剤として添加される塩素が反応して生じるトリクロラミン(NCl3)やN-クロロアルドイミンであるとされる。水道水のカルキ臭に関する分析法には,官能試験による臭気強度の測定や,ヘッドスペースGC-MS法によるトリクロラミンの分析がある。カルキ臭の制御を考える場合これらの分析に加えて,その前駆体であるアミノ酸やアンモニウムの分析も重要である。本稿では,我々の研究チームで行っている低濃度域でのアミノ酸とアンモニウムイオンの分析について紹介する。最初にそれぞれの分析法自体を紹介し,その後少しだけ苦労話を述べたい。
■まずアミノ酸であるが,HPLCの設定自体や反応試薬自体は,Prominenceアミノ酸分析システムの基本設定そのものを利用している(o-フタルアルデヒドによる誘導体化法)。ただし,測定にあたっては,遊離アミノ酸と結合アミノ酸両方を測定している1)。遊離アミノ酸とは他の化合物と結合をしていないアミノ酸を指す(普通のアミノ酸)。結合アミノ酸は総アミノ酸から遊離アミノ酸を差し引いたものである。総アミノ酸とは遊離アミノ酸に加えてペプチド結合やタンパク質等のアミノ酸同士で結合したものや腐食物質等の他の物質と結合したものを構成するアミノ酸の合計を指す。遊離アミノ酸については,感度確保のため前処理として試験管エバポレータで40 ℃にて,5倍に濃縮した。総アミノ酸については,前処理として6 M塩酸で20 時間,110 ℃で加水分解を行い,構成する遊離アミノ酸として測定を行った。遊離アミノ酸の定量下限値はグリシン,セリン,フェニルアラニン,β-アラニンが0.03 µM,それ以外の遊離アミノ酸が0.05 µM付近であった。
■図1に分析結果の一例を示す。限られた測定結果ではあるが,環境水や下水処理水中のアミノ酸は,ほとんどが結合アミノ酸の形態をとること,濃度範囲は数 µMから10数 µMであることがわかる。
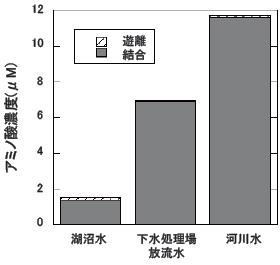 図1 環境水中アミノ酸の測定例
図1 環境水中アミノ酸の測定例
■次にアンモニウムイオンであるが,水道原水中には,数~数10 µg/L程度で存在していることが多い(場合によっては100 µg/Lを超えることもある)。数10 µg/L が一般的なアンモニア電極の検出下限であるが,それ以下であっても臭気閾値を超過するトリクロラミンが生成されるため,カルキ臭からみたアンモニウムイオン濃度の把握のためにはもう一桁低いレンジの分析が必要となる。一方で水道原水には,mg/Lオーダーのナトリウムイオンが共存する。ナトリウムはアンモニウムイオンとの分離が困難で,ごく微量のアンモニウムイオンを測定するためには,アンモニウムイオンに選択的な検出方法が望ましい。
■そこで,アミノ酸の場合と同様にo-フタルアルデヒドを誘導体化試薬に蛍光検出器を用いて測定することとした。測定条件はKuoらの方法を参考にした2,3)。分析条件を表1 に示す。図2に誘導体化による測定例,比較のために電気伝導度検出器による測定例を図3に示す。前者の方が明らかにナトリウムイオンの影響が小さいことがわかる。この後,この方法により1 µg/L付近でも十分なシグナルを得られることを確認した。
 表1 アンモニウムイオンの分析条件2,3)
表1 アンモニウムイオンの分析条件2,3)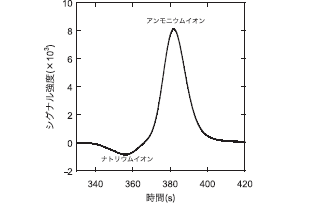 図2 ポストカラム誘導体化- 蛍光光度検出によるクロマトグラム
図2 ポストカラム誘導体化- 蛍光光度検出によるクロマトグラム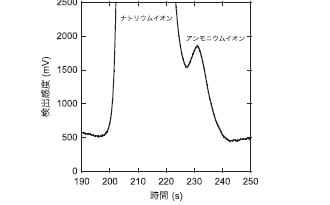 図3 電気伝導度検出によるクロマトグラム
図3 電気伝導度検出によるクロマトグラム■さて,これでめでたしめでたし,浄水プロセスの処理性の研究をしようということになるはずだったのだが,何度か分析を繰り返していると測定日によってどうもブランク値や標準試料に対するレスポンスが振れることがわかった。試薬の中の不純物や,ガラス器具の洗浄不足も疑ったが,結局はこのコンタミの主な原因は実験室内空気中のアンモニアであった。極端な例では,ビーカーに超純水を入れて,数時間放っておくと100 µg/Lを超えることもあった。それで,アンモニア濃度が低い実験室を探すことになり,ビーカーをあっちこっちにおいて実験室フロア全体のアンモニアマップが作れるくらいの分析をした。水の研究をしているつもりが,空気中のアンモニアの分析をするはめになったわけである。
■そのような試行錯誤があり,最終的に行き着いた解決法は以下の2点である。まず,試料の保存容器のキャップを全て密閉性の高いもので統一した(どのキャップがいいのかという「キャップの研究」も行った)。これで,保存中のコンタミは激減したのだが,実験操作を行う時にはどうしても大気と触れる。そこで,アンモニアフリーチャンバーなるものを特注で作ってもらった(これも島津製,写真1)。仕掛けは単純で,外部から空気を取り入れ活性炭フィルターを通しアンモニアを除去した空気をチャンバー内に送るものである。これにより,実験作業中のコンタミも激減し,ようやく安心して分析・実験ができるようになった。
 写真1 アンモニアフリーチャンバー
写真1 アンモニアフリーチャンバー■だいぶLCの話からは脱線してしまったが,アンモニアのように単純な物質の分析の方がかえって難しい場合があることや,水の研究をしていても空気中の物質が問題となることがあるという一例として紹介した。何かのご参考になれば幸いである。
参考文献