
LC分析の留意点

花井 俊彦 先生
公益財団法人 体質研究会 (ご所属・役職は2021年4月発行時)
1974年京都大学工学部助手として「非水溶媒クロマトグラフィーに関する若干の研究」で博士号を取得以来,ノースイースタン大学(ボストン),コロラド大学(ボールダー,コロラド),モントリオール大学(モントリオール,ケベック,カナダ)でポスドク,研究助手として10年過ごした後帰国。体質研究会研究員として,北里大薬では学生の研究を助けながら,真の博士号として,「分子間相互作用の定量分析」として,クロマトグラフィーの保持機構の定量解析及び生体機能解析への応用研究を継続。計算化学を用いる分析化学を配信中。
【専門分野】分析化学
【将来の夢】地球が死ぬまで好きなアメリカ,カナダと日本の旅を続けられたら
【趣 味】季節の訪れに合った美味しいものを料理して食する
■In silico chromatographyとは計算機を使ってコントロールするクロマトグラフィーでもクロマトグラフィーの結果を処理する意味でもない。過去に記録計からインテグレーターに変えた時に,保持時間だけでなくピークの高さや面積も打ち出してくれた時の喜びとは異なり,実験者が計算機と対話しながら化学を考えるクロマトグラフィーと捉えることができる。つまり,単に統計処理をするのではなく,データ集の中から読みだしてくれるシステムでもなく,化合物の特性を計算して教えてくれるシステムである。化学を考える(計算する)計算化学は有機化学の授業では早くから取り入れられ,2分子が近づくと電子の移動が起こり,2つの異なる分子として離れる動画も作られている。つまり,化学実験の可視化に使われるのが計算化学であり,定性的に想像していた化学現象を可視化して理解し易くするだけでなく,結果を数値の違いとして打ち出してくれるので,現象面を定量的に理解することを助けてくれる。分析化学において指示薬の色の変化を指示薬の構造変化とpHを変えて測定したスペクトルを比較して教えることが,化学現象を可視化した説明の最初と考えられるが,液体クロマトグラフィーの初期には植物からの抽出物が充塡ガラスカラムを通すと分離した異なる色の層として観察されたことから色グラフと称した。但し,色の化学構造との対比はされていない。
■クロマトグラフィーのカラム内における相互作用を化学構造から可能性で定性的に説明してきたが,説明に使われている相互作用の寄与程度を説明していない。近年,話題となった親水性相互作用によるクロマトグラフィーの説明がすっきりしないのも基本的な現象を定量的にとらえていないので,それぞれの寄与の程度が解らないことによる。親水性相互作用液体クロマトグラフィーの現象は高速液体クロマトグラフィーの初期から報告されていて,逆相分配液体クロマトグラフィーと称されていた実験で,有機溶媒濃度を濃くしていくと,短くなってきた保持時間が長くなりだす現象を,<多分,水素結合によるのではないか?>と推論しても,溶離液に水を含むので,<あり得ないのでは?>と話題にしていた。この現象の明確な説明は,計算化学を使って,モデル分子間の相互作用を調べると定量的にできる
■次に,水溶液中ではカルボン酸は解離定数からpHが3.5以下で分子型,pH 5.0以上ではイオン型,アミンはpHが9.5以下ではイオン型で存在することを踏まえて,これら分子間の水溶液中での挙動を2分子の一方は充塡剤の保持基,もう一方を溶質分子と見なして考える。例えば,図1において,構造A(赤:酸素,青:窒素,黄色:炭素,白色:水素)に示すように,イオン化したカルボン酸とアミンのイオン同士を7 Åの距離で向かい合わせて構造最適化すると構造Bのようにイオン同士が接する。表1のA→Bの分子間相互作用エネルギー値から,構造Aの2分子が独立した状態から接した構造Bになると,静電気(ES)相互作用エネルギー値7.149 kcal·mol-1が生じ,水素結合(HB)及び疎水性相互作用の指標であるファンデルワールス(VW)エネルギー値はそれぞれ0.000と0.260 kcal·mol-1であることから,これら2分子はES相互作用,つまり,イオンーイオン相互作用で接していることが解る。イオン化したカルボン酸とアルコールを6 Åの距離に近づけて(構造C),構造最適化(構造D)するとC→Dの分子間相互作用エネルギー値からES相互作用(2.849 kcal·mol-1)で接することが解る。分子型のカルボン酸とイオン化したアミン(構造E)は構造FのようにES相互作用(2.411 kcal·mol-1)で接するが,分子型アミンとイオン化したカルボン酸のアルキル基同士を3 Åの距離に近づけて構造最適化すると,弱いVWで接することが解る(0.635 kcal·mol-1)。強いイオンーイオン相互作用の場合と違って,VWのように相互作用が弱い場合には2分子を近づける必要がある。
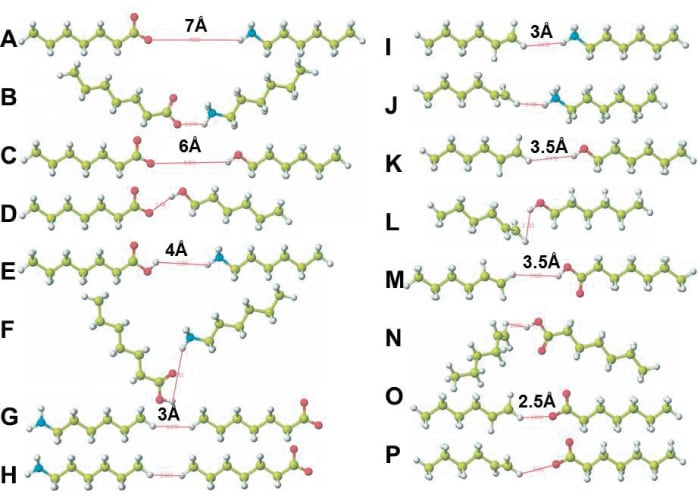 図1 簡便な分子間相互作用モデル
図1 簡便な分子間相互作用モデル表1 分子固有相互作用によるエネルギー値の変化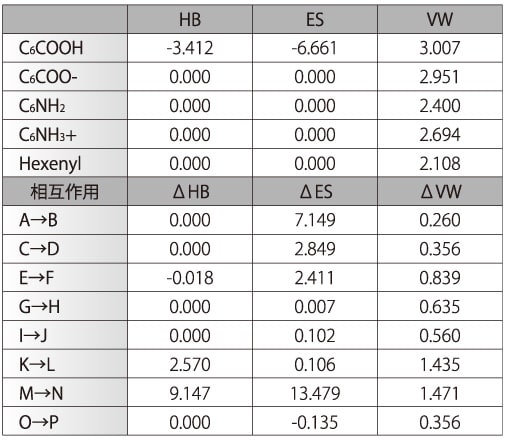
■ヘキシニル基を基準にして,イオン化したアミンと3 Åで向かい合せて(構造I)構造最適化すると2分子間の距離が縮まり,VW 値0.560 kcal·mol-1で接する。アルコールと3.5 Åの距離で向かい合せて構造最適化すると(構造K),HB およびVW 値が2.570 及び1.435 kcal·mol-1であることから,主たる相互作用はHBであることが解る。カルボン酸と3.5 Åの距離で向かい合せて構造最適化すると,HB及びES値が9.147及び13.479 kcal·mol-1であることからカルボン酸はHB及びES相互作用で接することが解る。更に,イオン化したカルボン酸と2.5 Åの距離に近づけて向かい合して,構造最適化すると,これら分子は反発し合って距離が2.9 Åと広がるだけでなく,ES値はマイナスになる。これらの計算で用いた2分子間の初期距離は2分子が接して構造変化をきたした距離で,2分子間の距離が長いと,これら2分子は近づく(相互作用する)ことなく,初期状態を保つ。
■相互作用エネルギー値で説明できる利点は,今まで相互作用の説明に使ってきた用語をファンデルワールス力,水素結合,静電気相互作用の3つのエネルギー値として説明できることで,静電気相互作用にはパイーパイ,ダイポールーダイポール,電荷移動型錯体形成とルイス酸塩基にイオンーイオン相互作用が含まれ,イオンーイオン相互作用の場合には静電気相互作用エネルギー値が大きい。実際にクロマトグラフィーの結果を定量的に論じるにはモデル相を構築する必要があり,充塡剤の表面構造が解かっていないので,予想モデル相を構築せざるを得ない。この為に実験値の保持比log k 値と計算で得られる相互作用エネルギー値との相関が理想とするほど高値を得られない場合があるが,全体としてどのようなことが起こっているかを把握するのには問題がない。誤差は生化学実験と違って,クロマトグラフィーは物理化学実験であり,保持時間の再現性が良い反面,計算に用いるモデル相が完全からほど遠いことに起因する。更に,脱離の主役である溶媒との相互作用(溶解度)も理解する必要がある。完全解を得る計算機プログラムの完成を待っていたのでは進歩がないので,どこまでできるのかを挑戦するのが化学者の意思である。
■解り易い低分子間の挙動を理解することになれたら,複雑な光学異性体認識基を構築して,光学異性体の認識,更に蛋白質の基質認識の違いを定量的に解析できるようになる。計算化学の利用は分離分析条件を検討するだけでなく,酵素反応の定量解析もできる自己学習である。幅広い化学現象を取り入れている分析化学に,有機化学で使われている学習法を取り入れ,慣れれば生物化学の学習もする。今後は無機化学の学習にも使われるであろう。
参考文献