島津製作所グループ受託分析会社 島津テクノリサーチ
- PIC/S GMP,ER・ES規制,CSV対応トータルソリューション
- 世界に深く浸透した島津製作所だからこそできる,PIC/S,FDA,厚生労働省対応ソリューション
- 島津の規制対応ネットワークシステム
- マルチデータレポートによる規制対応
- お客様に最高のソリューションを提供する 島津のクロマトグラフデータシステム
- 規制対応への充実したサポート
- バイオ医薬品測定装置Aggregates Sizerの例
- 島津製作所グループ受託分析会社 島津テクノリサーチ
島津製作所グループ受託分析会社 島津テクノリサーチ
- CRO(Contract Research Organization)complying with 21 CFR Part 11-
島津製作所のグループ会社として長年培った分析技術の経験を生かした事業を展開。
(株)島津テクノリサーチとして,医薬品安定性試験や薬物動態解析用分析・先端科学などの受託解析でお客様に正確で迅速なデータ提供を行っております。
生体試料中薬物濃度測定 -国内GLP(厚生省令21号)に準拠-
血・尿などの生体試料中微量成分の測定は,化学分析全般にわたる総合的な技術力が問われる難易度の高い分析です。
特に,新薬の開発研究に伴う非臨床試験や,フェーズ I を初めとする臨床試験で必要とされる薬物動態解析関連の分析は,薬物投与量・試料採取量の微量化やマトリックスの複雑化に伴い,年々その技術的要求は高まっております。
当社ではクロマト分析で長年培った前処理技術を始めとし,分析手法の開発からバリデーション・実試料の測定までを迅速に行い,正確なデータをお客様にお届けすることができます。
現在はGLP に準拠した濃度測定の受託も実施しております。

ご利用方法
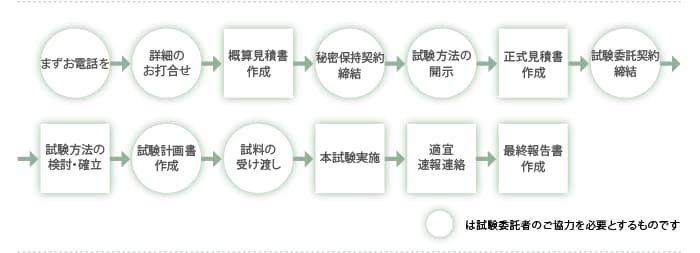
お問い合わせ先
|
株式会社 島津テクノリサーチ
|
|
| ■本社営業部(京都市中京区) TEL (075)811-3181 FAX (075)821-7837 |
■東京事業所(東京都大田区) TEL (03)5703-2721 FAX (03)5703-2740 |
| http://www.shimadzu-techno.co.jp/ E-mail:str_mado@shimadzu-techno.co.jp |
|
当社にて実施させて頂きました医薬品安定性試験の採取データが,米国向け新薬申請用資料として使用され,FDAによる申請事前査察〔PAI〕の調査対象に選ばれました。そして2003年夏,試験受託機関〔CRO〕としては国内初となる「FDAによる査察」が実施され,c-GMPに適合との評価を得ました。
医薬品安定性試験
-PIC/S GMPガイドライン 安定性監視プログラム-
-米国FDA 21 CFR Part 58(米国GLP)及びPart 11に準拠-
新薬開発や剤形変更に伴う,医薬品の安定性試験を受託しております。
当社は1989 年から安定性試験の受託業務を開始し,今日までに多くの実績を重ねてまいりました。既に,厚生労働省への申請が完了した医薬品も多く,年々受託試験件数も増加しております。医薬品メーカーが安定性試験を委託されるメリットは
- 当社が充分信頼に足る技術と組織を保有している。
- 委託料金が自社内で同様の試験を実施される予算とほとんど差がない。
- 年間計画からはずれた,突発的な企画の対応に便利である。
- 機器の管理や専門教育など,社内新設・増設と比較して経費面・組織面での問題が発生しない。
- 人員の有効利用が可能になる。
などが考えられます。
ご遠慮なくご相談ください。




