紫外可視吸収と有機化合物の構造との関係
染料や色素などに代表されるように有機化合物には着色したものが多く存在します。 これらの色はいったいどのようにして生じるのでしょうか。 色と有機化合物の構造との間には密接な関係があります。 ここでは当社の紫外可視分光光度計UV-2550を用いて測定した有機化合物の吸収スペクトルを基にしてその関係を説明します。
1.共役二重結合系と吸収ピークの関係
有機化合物には二重結合が一つおきに連なった共役二重結合(以下“共役系”とします)を持ったものが多く存在します。 この共役系がピーク波長と吸収強度に大きな係わり合いを持っています。
図1にベンゼン,ナフタレン,アントラセンの構造を,図2にそれらをエタノールに溶かして測定した吸収スペクトルを示します。 図2は各成分の吸収強度がほぼ同じになるように濃度を調整して測定しました。図2から共役系が大きくなるほどピーク波長は長波長側にシフトすることが分かります。 表1 1) に種々の有機化合物のピーク波長とモル吸光係数を示しました。 モル吸光係数は物質が光を吸収する度合を示す指標で値が大きいほど強い吸収となりますが,共役系が大きくなると吸収ピーク波長が長波長側にシフトすると共に吸収ピークも大きくなることがわかります。
| 物質 | 吸収ピーク | モル吸光係数 |
| エチレンCH 2 =CH 2 1.3-ブタジエン ビタミンA β-カロチン |
180nm 217nm 328nm 450nm |
10000 21000 51000 140000 |
| ベンゼン ナフタレン アントラセン ナフタセン |
255nm 286nm 375nm 477nm |
180 360 7100 110000 |
図1 ベンゼン,ナフタレン,アントラセンの構造
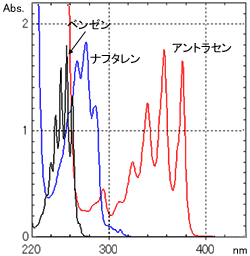
図2 ベンゼン,ナフタレン,アントラセンの吸収スペクトル
2.共役系が大きい食用色素の吸収スペクトル
図3に食用色素の赤色102号と青色1号の構造を,図4に赤色102号と青色1号の吸収スペクトルを示します。 食用色素は一般に図3のような大きな共役系を持っているためにピーク波長は大きく長波長側にシフトし,可視域(400nm~700nm)にピークが現れるために色として認識されます。
ところで,我々が見る色は物質に吸収されなかった残りの色(補色または余色と言う)です。 赤色102号は図3に示すように450nm~550nmの青,緑色系統の光を吸収するので,補色の赤色が目に入ります。 青色1号は560nm~650nmの黄色系統の光を吸収するために青色として目に映ることになります。
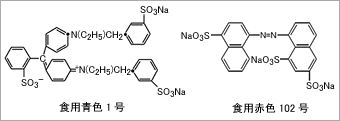
図3 赤色102号と青色1号の構造
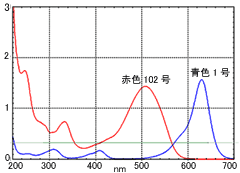
図4 赤色102号と青色1号の吸収スペクトル
3.官能基の影響
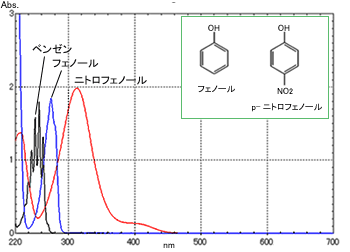
図5 ベンゼン,フェノール,p-ニトロフェノールの吸収スペクトル
官能基によっても吸収ピークは影響を受けます。 ベンゼン,ベンゼン環に-OH基が付いたフェノール,ベンゼン環に-OH基と-NO2基が付いたp-ニトロフェノールの吸収スペクトルを図5に示します。 官能基が共役系に影響を与えるために吸収ピークがベンゼンよりも長波長側に現れますが,400nm以上の可視域まではシフトせず,有機化合物の色は共役系の大きさの方が大きな影響を及ぼしています。
4.分子骨格は大きいが共役系が小さい化合物の吸収スペクトル
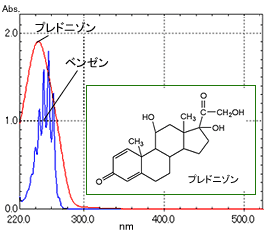
図6 プレドニゾン,ベンゼンの吸収スペクトル
医薬品として用いられるプレドニゾロンとベンゼンの吸収スペクトルを図6に示します。 プレドニゾロンは大きな分子骨格を持ちますが,共役系が小さいためピーク波長は長波長側に大きくシフトせず,ベンゼンとほぼ同じ位置に現れています。
5.長波長側にシフトする理由
分子構造と吸収スペクトルとの関係を示してきました。 共役系が大きいとなぜピーク波長は長波長側にシフトするのでしょうか。 光のエネルギーと電子の運動との関係で考えてみましょう。
光は波と粒子(光子)の二つの性質を持ち,1個の光子のもつエネルギーはhc/λで表されます。 ここで,hはプランク定数,cは光速度,λは波長です。
紫外可視域の吸収は電子の遷移に関係しています。 電子の遷移とは電子の運動状態が別の運動状態へと変わることです。 共役系のπ電子は分子の骨格を形づくっているσ結合の電子より運動状態が変化しやすい性質をもっています。 このようなπ電子に光子が衝突するとその運動状態は簡単に別の運動状態に変えられてしまいます。 エネルギーの小さい光子でも,π電子ならば比較的簡単に運動状態を変えてくれるのです。 共役系が大きくなればなるほどπ電子は小さなエネルギーの光子の影響を受けやすくなります。 遷移は光子のエネルギーが電子に吸収されたことを表しています。 光子のエネルギーが小さいということはhc/λが小さいことを意味し,これはλが大きいことを意味します。 λが吸収波長となりますので,共役系が存在すれば,λが大きい領域,すなわち長波長側にピークが現れるということになります。
参考文献
1) 中原 勝儼:「色の科学」,培風館(2002年),P108



