2.気泡発生のメカニズム
2-3)異なる溶媒の混合
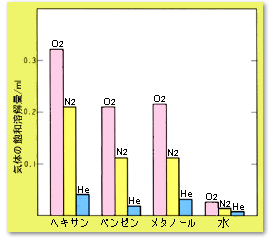
気体の飽和溶解量は,液体の種類によって異なります。 概して,極性の低い気体は,極性の低い溶媒に溶けやすくなります。 図5では,ベンゼンとメタノールへの体積当りの気体の溶解量がほぼ同じことを示していますが,これを溶媒のモル数当りの溶解量,つまりモル分率で計算すると,溶媒の極性が低いほど溶解度が高いことが鮮明になります。
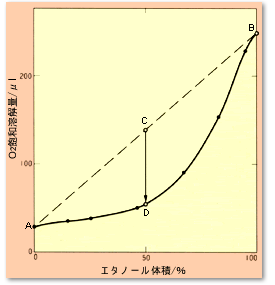
それでは,異なる溶媒を混合すると飽和溶解量はどうなるのでしょうか?答えは,単独溶媒の溶解量の和に比べて小さくなる,というのが一般的です。 図6に,水-エタノール混合溶液へのO2溶解量(分圧1気圧)を示しました。 A点は水100%への溶解量,B点はエタノール100%への溶解量です。 水とエタノールを同量混合した時には,C点に相当するO2が溶液に存在するわけですが,この溶液の飽和溶解量はD点しかないため,C→D相当のO2が気泡として発生することになります。 同じようなことが,水-メタノール,水-アセトニトリルへの空気の飽和溶解量にもみられます。
* 1気圧(1atm) = 1.013×105Pa
 |
||
|
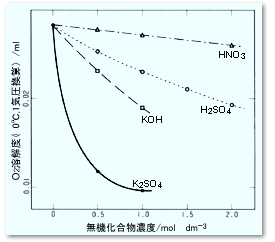
また,混ぜる溶媒が水同士であっても気泡発生が生じる場合があります。 というのは,一般に塩濃度が上がると空気の飽和溶解量が下がるが,その関係は直線的ではなく図7のように下に凸の曲線を示す場合があるからです。
 |
||
|
 |
||
|
| <参考文献> | S.R.Bakalyar,M.P.T Bradley and R.Honganen,J.Chromatogr., 158,277-293(1978) |
| 化学便覧 基礎編II 8.7溶解度,日本化学会編 丸善株式会社(1984) |