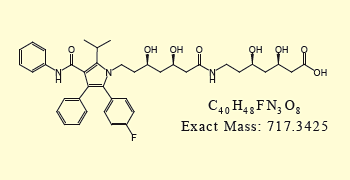トラップフリー2次元LC/MSシステム - アプリケーション
四重極型LCMS用
医薬品の安全性向上を目的として,医薬品中に含まれる不純物の遺伝毒性など重篤な毒性の有無を解析するために構造解析が求められています。微量不純物の構造解析にはLC/MSを活用することが有効ですが,一方で,HPLCによる不純物の一斉分析では210nmなどの短波長で検出するため,移動相緩衝液にりん酸緩衝液を使用することが多くあります。このような場合,その分析条件のまま未知不純物をLC/MSに導入することは困難です。また,緩衝液のpHを同一にしても,その種類により分離状態が変化することがあり,目的の未知不純物をLC/MSで確実に解析することは困難です。
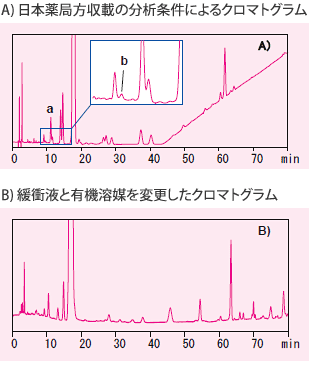
図1はアトルバスタチンカルシウムの不純物分析について,移動相緩衝液を日本薬局方収載のくえん酸緩衝液 pH5.0(不揮発性塩であるためにLC/MSへの導入が困難)から,同一pHの酢酸緩衝液に,有機溶媒をテトラヒドロフラン/ アセトニトリル(1/1)混液からアセトニトリルに変更した際のクロマトグラムです。主成分の溶出時間には大きな違いはありませんが,不純物の溶出パターンが大きく変わっていることがわかります。
従って,不純物の構造解析のためには,LC分析条件の移動相のままで,目的の不純物をLC/MSに導入する必要があります。
ここでは,“トラップフリー2次元LC/MS不純物同定システム”(図2)をこれらの不純物構造解析に活用した例をご紹介します。
本システムの1次元目では,通常のHPLC分析条件で分離し,構造解析を行いたい不純物ピークのピークトップ付近をピーク捕獲ループに導きます。このループは,2次元目の分離に対してインジェクタの役目を果たします。2次元目は,1次元目の移動相成分と目的不純物の分離およびLC/MSへの導入の役目を果たします。
従って,2次元目の分離条件は個別検討を行うことがほとんどなく,一般的な0.1%ぎ酸/ アセトニトリルによるグラジエント溶離を用いMSに導入します。また,MSには構造解析のために精密質量数が得られ,MSnが可能なLCMS-IT-TOFを使用しています。
![図2 トラップフリー2次元LC/MS不純物同定システムの構成 [1次元目(赤の流路)は通常の分析条件で使用]](/sites/an.shimadzu.co.jp/files/ckeditor/lcms/c6nq2v000002yxhd-img/c6nq2v000002yxzv.jpg)
[1次元目(赤の流路)は通常の分析条件で使用]
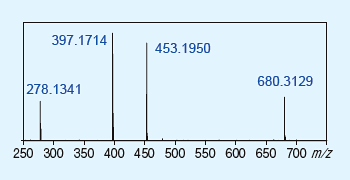
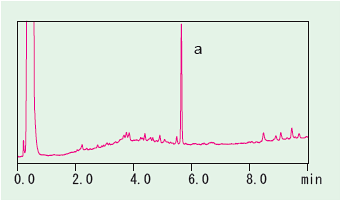
図3に,日本薬局方収載の分離条件で検出された不純物a(約0.2%含有,図1参照)について,2次元目のクロマトグラムを示します。トラップ濃縮を行わず,ピークトップ付近を2次元目に導入することで,1次元目のシステム由来成分の影響を抑制し,目的不純物をMSに導入できていることがわかります。図4に,この不純物に対して得られたMSスペクトルを示します。
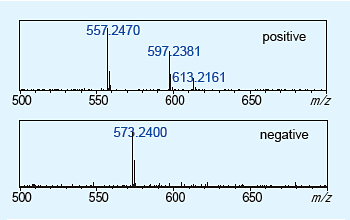
ポジティブイオンとネガティブイオンを同時に検出することにより,分子由来の質量数を検出できていることが確認できます。
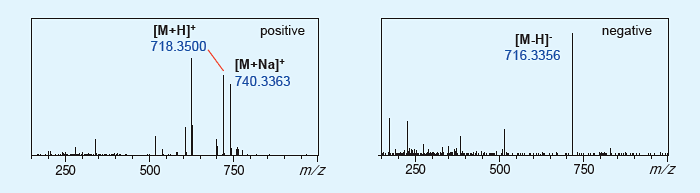
さらに,不純物aで得られたm/z718のイオンについてMS/MSスペクトルを得た結果が図5です。本スペクトルを主成分であるアトルバスタチンのMS/MSスペクトルと比較することで,不純物aの構造は図6と推定されました。さらに,より微量な不純物b(約0.01%,図1参照)についても図7の通り,ポジティブ,ネガティブ両方のマススペクトルを優れたS/N比で得ることができました。