カラムを用いて分離する 〜カラムを用いて適切なピークが得られることを確認する〜
LCtalk62号in the LAB
LC-MSの分析条件について(その2)のフローインジェクション分析(FIA)では,1) なんらかのイオンが生成していること,2) そのイオン質量が目的化合物に関連するものであることをチェックし,目的化合物がLC-MS分析(=質量分析検出)可能であるかどうかを確認しました。 今回はカラムを用いても適切なピークが得られるかの確認と,適切にピークが得られなかった場合の対策について説明します。
カラムを用いたフローインジェクション様分析
クロマトグラフィーは,目的により分析時間が長くなってしまうこともよくありますが,検討段階ではできる限り時間短縮を図りたいものです。 このような場合,ハイスループット分析に対応できる汎用カラム(たとえば,Shim-pack FC-ODS,長さ 75 mm×内径 2.0 mm)を用いることにより検討時間を短くすることができます。 つまり,移動相の流速を通常の 2~3倍に相当する 0.4~0.6 mL/minに,移動相の有機溶媒比率を高く設定することにより,目的化合物を速やかに溶出させます。(A: 0.1 %ぎ酸水溶液,B: アセトニトリル,のときA/B=1/9で始めてみる。) ここでは,これをFI様(フローインジェクションよう)分析と呼びます。
このFI様分析のチェックポイントは,
(1)目的化合物がカラムを通過できるか?
(2)目的化合物のピーク形状は良好か?
(3)目的化合物のマススペクトルパターンに変化はないか?
の3点です。 (1)目的化合物がカラムを通過できるか?
ほとんどの化合物を速やかに溶出させる条件なので,目的化合物はおそらくカラムを素通りするだけでFI分析のようなピークが確認されます。
(2)目的化合物のピーク形状は良好か?
(1)と同時に確認できることが,目的成分のピーク形状です。 逆相系の分離条件を前提としているため,この条件でピークの形状が悪いようでは(主にテーリング),目的成分の保持・夾雑成分との分離考慮した最終的な条件で満足できる結果が得られないことが容易に予測できます。
(3)目的化合物のマススペクトルパターンに変化はないか?
マススペクトルはFIAですでに取得していますが,A)目的成分が移動相と十分混合するため,またB)カラムを通過させることにより試料溶液に含まれる塩の影響を小さくすることができるため,スペクトルパターンが変化することがあります。
FI様分析では,実際に用いるクロマトグラフィー分離場でのスペクトルパターンを見ることができます。 スペクトルパターンに大きな違いがないか?(=観察されたイオンの帰属が可能),使用する移動相条件でどのようなイオン種が優位になるかを確認します。
この検討過程も,ほとんどの化合物では問題なくクリアできるはずですが,極まれにこの過程で問題が起こることがあります.その対策について少しふれます。
(1)カラムから溶出しない
強い疎水相互作用を示す化合物はアセトニトリル/水(=9/1)で溶出できない化合物も出てきます。 トリグリセライドやクロロフィルなどは,この条件で速やかにカラムを通過させることはできません。 この場合には大幅な条件検討が必要になります。
つまり,1) より溶出力の高い移動相であるアセトンやメタノール・イソプロパノール混液に移動相を変更する(逆相系分離を前提とした対策)。 別の方法として,2) 異なる分離モード(順相系など)を検討することがあります。 しかし,順相系でよく用いられる移動相はヘキサン,ベンゼン,クロロホルム,酢酸エチルなど大気圧イオン化に適さない溶媒であるため,単純に順相系のカラムや移動相への交換だけではLC-MSには適用できません。 イオン化に都合の良いメタノール,アセトンなど(基本移動相)が移動相として加えることができるかどうか?がLC-MS分析に適用できるかの鍵となります。
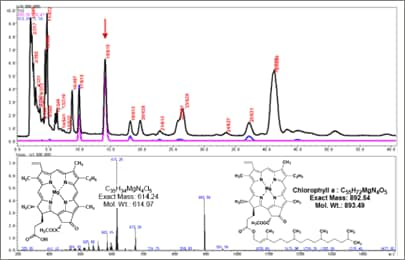
(ヘキサン/アセトン 88:12)
実際に,ヘキサン/アセトン(8/2),ヘキサン/エタノール(7/3),クロロホルム/メタノール(95/5) のような移動相を用いて順相系LC-MS分析を行った例は多々あります(図1)。 ただし,基本溶媒の割合が低くなるため,感度や安定性が低くなるなどの デメリットが有りますが,分離のメリットが勝る場合にはこの解決法が選択されます。 この場合移動相の大幅な変更を伴うため,はじめに戻って"FIAによるイオン化,イオン化法の確認および観察されたピークの帰属"を行う必要があります。
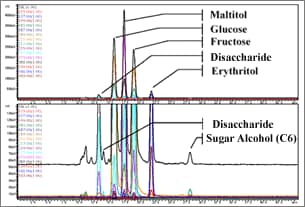
LC-MS分析はカラムや分離モードを制限するのではなく,移動相を制限する分析法と考えてよいでしょう。 配位子交換モードによる糖質の分析(図2)では,移動相は水しか使用しないことからLC-MS分析に適した分析といえます。
(2)ピーク形状が悪い
カラムを用いたFI様分析で,たまにピークテーリングが観察されることがあります。 この場合,移動相pHを少しふってみます。 この分析条件では,ぎ酸を加えた水を用いていますが,移動相BにはLC-MSの分析条件について(その1)でお話したように酸を加えていません。
そこで,有機溶媒比率を少し下げて同様の分析を行った場合に,ピーク形状の改善が見られるかどうかを確認するわけです。 逆相条件なので,有機溶媒比率を減らせば,保持時間は長くなりますが酸の影響で,ピーク形状が改善する化合物があります。 改善が見られる場合には,有機溶媒にも酸を添加した移動相に変更することで良好な結果が得られます。 オキソリン酸やニューキノロン系抗菌剤(サラフロキサシンのなど)がこれに相当します。
(3)マススペクトルのパターンを確認
先に示した理由によりFIAとは観察される分子イオン種が変わります。 未知化合物の同定では,様々なイオン種の出現が分子量決定に役立ちます(その2参照)が,定量分析を目的とする場合,イオン種をそろえる方が感度や安定性を高めます。
アセトニトリル-ぎ酸水系を用いた分析ですが,
A) アンモニウムイオン付加型分子(正イオン)が観察される場合*
ぎ酸をぎ酸アンモニウムに変更し,アンモニウムイオン付加型分子の強度を高めます。
B) 塩素イオン付加型分子(負イオン)が観察される場合*
塩素イオンの供給源として,移動相にまたはポストカラムで塩素系溶媒を添加します。
C) 負イオン分析で脱プロトン分子が観察される場合
ぎ酸を除く,ぎ酸アンモニウムを添加することで,移動相のpHを上げ,目的化合物の感度を向上させます。
D) ぎ酸イオン付加型分子が確認される場合
基本移動相条件でのぎ酸付加型分子の強度とぎ酸を含まない系での脱プロトン分子の強度比較をおこない良好な条件を選択します(単純なイオン強度ではなく,S/Nで判断することをお薦めします)。
*アンモニウムイオン付加型分子や塩素イオン付加型分子のアンモニウムイオンや塩素イオンの由来は,カラムや流路に残存していたものと考えられます。
第一選択移動相として用いた基本移動相は,塩基性化合物(正イオン分析)に適した条件であるため,酸性化合物が対象となる場合,いろいろと検討が増える傾向があります。 (Mu)
補足説明:過去の分析実績などから,目的化合物が適切に検出できると予想される場合は,移動相A,Bのグラジエント条件で分離できるかどうか確認することもあります。
LCMS, 液体クロマトグラフィー質量分析装置


