pHによるイオン性の変化

一般に,イオンクロマトグラフ(以下,ICと略)で分析対象となるのは,水中で電荷を持った状態で存在する元素イオンや低分子イオンです。(以下,イオンと略)
イオンは,無機イオン,有機酸,アミン類などいくつかに分類されます。
これらの中には存在する環境(pHの違い)によって,そのイオン性(電荷状態)が変化するものがありますのでIC分析でも十分な考慮が必要です。
そこで,IC分析の留意点の内で「pH」に焦点をあてて,いくつかの事例をご紹介したいと思います。
イオン分析には溶媒のpHが重要!
強酸,強塩基由来の一般的な無機イオンは,水中では完全に陰・陽イオンの形態で存在しています。ICで使用する移動相には,適当な溶出力を持たせるため,酸や塩基を組み合わせて使用します。通常pH3~pH11程度であり,試料をICに注入した場合でも,ほぼ完全に解離した状態で安定して分析する事ことが可能です。
有機酸・アミン類(アンモニウムなど)はそれぞれ固有の酸解離定数(pKa)をもっています。これらの物質は,溶媒のpHや試料濃度により解離(イオンの状態)・非解離状態の平衡が変化するため,ICで検出可能な“イオンの状態で存在”する率が変化します。分析条件や分析(検出)方法によっては検量線の直線性が得られない場合があります。
イオンクロマトグラフの方式とpH
ICにはノンサプレッサ方式とサプレッサ方式の2種類があります。これらはサプレッサが単にあるかないかというハードウェア構成の違いとは別に,化学的な意味での違いがあります。それぞれの場合を例にとって説明します。ノンサプレッサ方式では,通常移動相として,弱酸の緩衝液や酸の水溶液を用います。調製された移動相の組成は分析カラム内でも検出器セル内でも変化せずpHも変化しません。分析対象イオンは,移動相の緩衝能やpHにより完全に解離した状態で分離・検出されるため濃度と伝導度が直線的な相関をもちます。
サプレッサ方式の場合は,移動相のバックグランド伝導度を低減するため,検出器の直前で目的イオンと対イオンとなるイオンを除去するので移動相組成が分離時と検出時で異なります。この組成の変化はpHの変化となるため,特に有機酸やアミン類(アンモニウムなど)を分析する場合にはその解離状態に影響するため注意が必要です。サプレッサ方式のICでアンモニウムイオンの検量線が曲がる現象は良く知られたことです。
アミン類の検量線には要注意!
アンモニウムは,
NH₃+H⁺⇄NH₄⁺
の平衡状態にあり,移動相のpHにより状態が変化します。 酸性条件下では平衡は右によるためNH4+の存在比率が増しますが,pHの上昇と共にNH4+ は減少します。 また,移動相pHが高い状態では,試料濃度が高くなるほど解離が抑制され,NH4+の存在比率が小さくなるため濃度とレスポンスが比例しなくなり検量線が曲がるという現象が発生します。
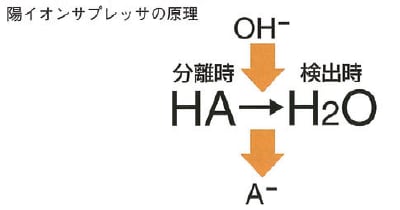
陽イオンサプレッサでは,移動相として硫酸やメタンスルホン酸といった酸の水溶液を用いますが,サプレッサ内では,この中の硫酸イオンやメタンスルホン酸イオンをOHイオンに交換するため,サプレッサ溶出液は水(pH7)になります。
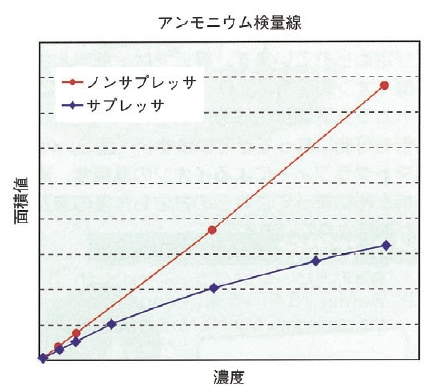
このため,上記の現象が起こり検量線が曲がることとなります。 この傾向は,サプレッサの効率が良いほど顕著に現れます。 当然,ノンサプレッサ方式では酸性移動相を使いますので,このような検量線の曲がりは発生しません。
有機酸の分析でもpHにご注意を!
陰イオンサプレッサ方式で,有機酸を分析した例をご紹介します。サプレッサ方式の移動相は炭酸ナトリウム/炭酸水素ナトリウム水溶液を用います。この場合の移動相pHは9以上ですので,有機酸はほぼ完全に解離した状態で分離されます。
この状態で検出器を通過すれば有機酸のほぼ全量をイオンとして検出することができますが,サプレッサでは移動相のバックグランド伝導度を低減するため,移動相中のNaイオンをHイオンに交換します。このため検出時の移動相(サプレッサ溶出液)は炭酸水となり,pH5~6程度の弱酸性となります。
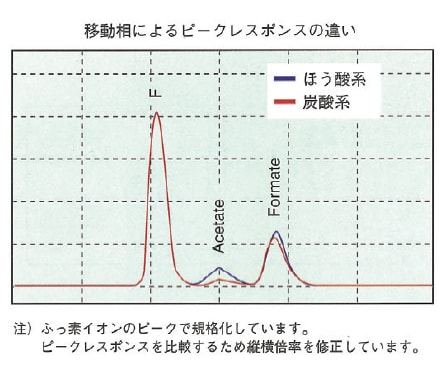
有機酸はカルボキシル基をもっているため pKa約4.5となり,検出時の移動相pHと近いため解離がある程度抑えられた状態となります。図は分析用の移動相として炭酸系とほう酸系の移動相をそれぞれ使用した場合の酢酸,ぎ酸のピークレスポンスの違いを示したものです。
ほう酸系移動相の場合もサプレッサ通過後はほう酸水となり,pHは6~7程度となります。ふっ素,酢酸,ぎ酸はそれぞれ同濃度の試料を用いています。ほう酸系移動相の方が,炭酸系移動相に比べ酢酸,ぎ酸のピークレスポンスが大きいことがわかります。また,ぎ酸より酢酸の方がレスポンス変化が大きいことがわかります。
これは,酢酸とぎ酸の pKaがそれぞれ約4.5,約3.5と異なるためです。移動相pHとpKaが離れるほど解離度が大きくなるため,炭酸系からほう酸系に変わることによるpHの変化をより受けやすいのは pKaの大きい酢酸ということになります。
(Ie)