
お客様のご意見・ご要望のご紹介

高垣 敦 先生
九州大学 大学院工学研究院 応用化学部門 准教授 (ご所属・役職は2022年4月発行時)
六方晶窒化ホウ素はグラファイトに類似した結晶構造を有する層状化合物であり,ホワイトグラファイトとも呼ばれている。一般的には化学的に不活性であり安定な化合物であるため,固体潤滑剤などに使われている。赤外分光では,試料の希釈にKBrを用いることが多いが,固体粉末のX線吸収微細構造(XAFS)を測定する際には,試料の希釈に窒化ホウ素を用いる。固体触媒に関する応用としては,その化学的安定性のためにこれまでは担体として利用することがほとんどであったが,近年窒化ホウ素そのものが優れた触媒作用を示すことが報告されている。代用的な例が低級アルカンの酸化的脱水素反応であり,窒化ホウ素を触媒として用いると,プロパンからプロピレンが,エタンからエチレンが効率よく合成できることが明らかにされた[1]。我々は,窒化ホウ素に適切な処理をすることで,高い表面積を有する新しい固体塩基触媒として機能することを見いだした[2]。アルドール反応,ニトロアルドール反応,クネ-フェナ-ゲル縮合,グルコース異性化反応などに活性を示す。赤外分光法により窒化ホウ素の構造と固体塩基性について評価を行ったので本稿で紹介する。
まず我々は結晶性の高い六方晶窒化ホウ素を粉砕処理した[2,3]。粉砕処理には遊星型ボールミル装置を用いた。層状構造を有している六方晶窒化ホウ素はボールミル処理により,層の剥離だけでなく,BNシートの部分的な破砕が生じ,その結果400 m2 g-1程度の表面積を有するようになった。ボールミル処理前後の窒化ホウ素のFTIRスペクトルを図1に示す。ボールミル処理前の窒化ホウ素は1376 cm-1と819 cm-1に吸収が見られ,それぞれB-N伸縮振動,B-N変角振動に帰属される。回転速度300 rpm以上でボールミル処理を行うと,これらのピークの減少だけではなく,いくつかの新しい吸収が観測された。1079 cm-1と925 cm-1の吸収はB-O振動に帰属できる。また,おおよそ3400 cm-1と3150 cm-1にブロードな吸収が観測された。これらはそれぞれO-HおよびN-H伸縮振動に帰属され,ボールミルの回転速度を上げるにつれて吸収は強くなっていった。ボールミル処理によって固体表面にアミノ基と水酸基が形成したことを示している。表面にこれら官能基が生成する理由としては,粉砕時に機械的な力が窒化ホウ素にかかり,その後空気中の水分と反応することで,骨格のB-Nが加水分解するためと考えられる。ボールミル処理の回転速度と表面積およびニトロアルドール反応との関係について図2に示す。300 rpm以上において表面積の大幅な増加が見られ,400 rpmにおいて最大値(412 m2 g-1)を示した。それ以上回転速度を上げると表面積が減少した。これは粒子が細かくなると,表面エネルギーが増大しむしろ凝集しやすくなるためと考えられる。ニトロアルドール反応については,FTIR測定においてアミノ基と水酸基が観測された300 rpm以上の試料において活性が見られ,400 rpmのときに最大活性を示した。
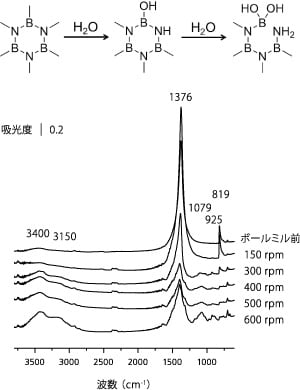
図1 ボールミル処理した窒化ホウ素のFTIRスペクトルとアミノ基,水酸基の生成過程
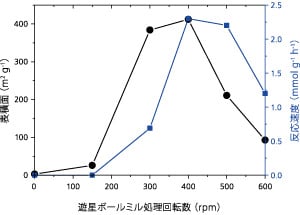
図2 ボールミル処理した窒化ホウ素の表面積とニトロアルドール反応活性
ホウ酸と窒素含有化合物を用いて,縮合化合物を経由し,熱分解すると多孔質の窒化ホウ素を合成することができる。ホウ酸と尿素を水に溶解させ蒸発乾固させ,得られた固体をアルミナボートに移し,アンモニア雰囲気にて1000°Cで加熱し,乱層構造(turbostratic structure)の窒化ホウ素を合成した[4]。この合成において,ホウ酸と尿素のモル比をホウ酸:尿素=1:2 から1:15 まで変化させて合成すると,表面積,細孔容積が大きく異なった。モル比1:2の場合は376 m2 g-1 の表面積を有したが,そのほとんど(370 m2 g-1)はミクロ細孔由来であった。一方,モル比を1:5 にして合成した試料は,約500 m2 g-1 の表面積を有し,メソ細孔を有した。細孔容積が合成した試料の中では最も多かった。モル比が1:10 の場合は,表面積はさらに高く647 m2 g-1 を示した。窒化ホウ素をボールミル処理した場合は,最大表面積が約400 m2 g-1であったのに対し,熱分解法により合成した場合は,さらに高い表面積が得られた。これらの試料のFTIR スペクトルを図3 に示す。高結晶性窒化ホウ素をボールミル処理した場合と同様に,アミノ基と水酸基による吸収が観測された。パラメトキシベンズアルデヒドとニトロメタンを用いたニトロアルドール反応の結果を図4 に示す。触媒活性は窒化ホウ素合成時のホウ酸と尿素のモル比に大きく依存した。ミクロ細孔のみのモル比1:2 の試料ではほとんど活性を示さず,一方で,モル比1:5の試料では転化率83%と最も高い活性を示した。同反応条件で代表的な固体塩基を用いた場合と比較すると,多孔質窒化ホウ素は良好な触媒活性を示すことがわかった。この試料の固体塩基性を評価するにあたり,まず古典的な指示薬法を用いた。ホウ酸と尿素を用いてアンモニア中で合成した試料は白色であり,指示薬による呈色を確認することができる。pKa = +6.3 のブロモクレゾールパープルを指示薬として用いたとき,固体表面が着色した。一方,フェノールフタレインでは着色が見られず,弱塩基性であることがわかった。指示薬法は簡便な方法ではあるが,対象試料が白色であること,指示薬の分子サイズが影響しないことなどの制限がある。また指示薬による着色後に酸による滴定をして固体塩基量を求めることもできるが,目視によるため一般に誤差が含まれる。
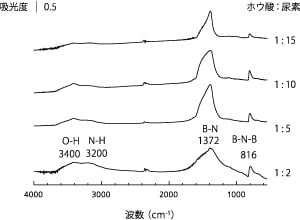
図3 ホウ酸と尿素を出発原料として合成した 窒化ホウ素のFTIRスペクトル
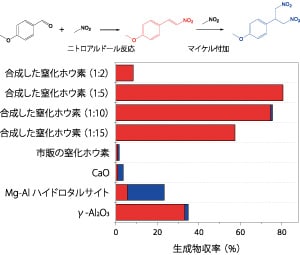
図4 ホウ酸と尿素を出発原料として合成した 窒化ホウ素によるニトロアルドール反応
プローブ分子を用いたFTIR測定は,触媒の固体酸塩基性を評価する代表的な手法である。硝子製のIRセルに試料をセットし,閉鎖循環系を用いて測定を行った。200°Cで真空加熱前処理後,室温にて飽和重クロロホルム(CDCl3)ガスを30分吸着させ,その後真空引きした後にFTIRスペクトルを得た。結果を図5に示す。スペクトルは吸着前後の差スペクトルである。クロロホルム中の重水素が水素結合を通して窒化ホウ素の塩基点と相互作用することで,2252 cm-1にC-D伸縮振動が観測された。文献によると,SiO2上では2265 cm-1,γ-Al2O3上では2253 cm-1,MgO上では2245および2220 cm-1に観測されており[5-7],比較すると,合成した窒化ホウ素の塩基点はγ-Al2O3と同程度であるが,MgOのように強塩基ではないことがわかった。
熱分解法による合成では,出発原料を選択することができる。第3級アミンであるヘキサメチレンテトラミンを窒素含有化合物として用い,ホウ酸と混合し,熱分解法により窒化ホウ素を合成した[8]。この試料も他の合成した窒化ホウ素同様にFTIRスペクトルを測定すると,3400 cm-1付近に水酸基,3200 cm-1付近にアミノ基に由来する吸収が観測された。合成した試料は構造内に酸素を有しており,黄褐色を示した。このため指示薬法による塩基性評価はできなかった。クロロホルムCHCl3をプローブ分子として吸着させ,FTIR測定を行った結果(差スペクトル)を図6に示す。気相のクロロホルムは3019 cm-1にC-H伸縮振動が見られるが[7],本試料では2984 cm-1にレッドシフトして観測された。加えて,3212 cm-1を中心とした負のピークと,3160 cm-1を中心とした正のピークが観測された。これは3200 cm-1付近に見られたアミノ基が塩基点として働き,クロロホルムのC-Hと相互作用したことを示している。2984 cm-1へのレッドシフト値を既報の触媒と比較すると,ヘキサメチレンテトラミンを用いて合成した窒化ホウ素の塩基強度は,SiO2,γ-Al2O3,NaXゼオライトよりは強く,KXやCsXゼオライトよりは弱いことが示された[5,9,10]。
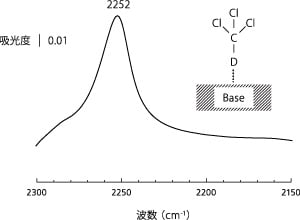
図5 CDCl3を吸着させた窒化ホウ素(ホウ酸と 尿素より合成)のFTIR差スペクトル
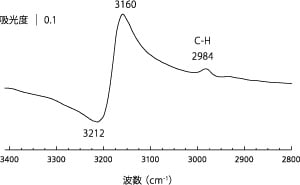
図6 CHCl3を吸着させた窒化ホウ素(ホウ酸とヘキサ メチレンテトラミンより合成)のFTIR差スペクトル
これまで触媒として利用されていなかった窒化ホウ素をボールミル処理あるいは,熱分解法により合成することで固体塩基触媒として応用できることを見いだしてきた。FTIR 測定を用いることで,合成した窒化ホウ素の構造や固体塩基性を評価できた。塩基性は弱いものの,実際の塩基触媒反応では高い触媒作用を示す。その理由として,固体表面に共存する水酸基の影響があげられる。基質の置換基効果による実験から,ニトロアルドール反応においては,酸塩基協奏作用により反応が進行していることが示唆されている[2-4]。
新規触媒材料を開発するにあたっては,その特性,触媒作用および反応機構を理解することが重要である。本稿では詳細を割愛したが,FTIR 測定以外にもXPS,固体NMR測定,軟X 線吸収微細構造(XAFS)測定をキャラクタリゼーションに用いている。群盲象を評す,という寓話にあるように,FTIR 測定をはじめとする種々の分析測定を行い,材料の多角的にとらえ,全体像を把握することが,その材料を正しく理解を深めることにつながると考えられる。
謝辞
上記の研究成果は,鳥居修作氏,難波翔一朗氏,菊地隆司准教授,S. Ted Oyama 教授(東京大学大学院工学系研究科(当時)),中村昇平氏,石原達己教授(九州大学大学院工学研究院)の協力のもとに得られました。心より感謝申し上げます。