
お客様のご意見・ご要望のご紹介

大塚 誠 先生
武蔵野大学薬学部・薬学研究所 (ご所属・役職は2006年8月発行時)
緒言
近年、製造物責任法(PL法)の施行により、製造した製品に関する規制は、厳しくなりつつあるが、医薬品製造工程においては、製造に関する規定(GMP)が厳格なことから製造技術の更新が保守的となり、技術革新が、かなり立ち遅れているのが現状である。このため、今まで以上の高い品質の医薬品を製造するために米国食品医薬品管理局(FDA)を中心にして、製造プロセスの進行中に、製品の重要品質パラメーターをタイムリーに測定し、プロセスの終了時点で最終製品の品質を保証する、製造工程の分析と管理、PAT(Process Analysis Technology)の実践と規制導入を模索している1-3)。製造工程の自動管理では、製造ラインに組み込んだセンサーによって製造ライン上の対象物の品質を非破壊的に分析し、この分析情報を製造ライン制御に瞬時にフィードバックすることが求められることから、迅速で正確な分析方法が要求される3)。このため、採用可能な分析法としては近赤外分光法(NIR)4-9)およびラマン分光法10)などの非破壊・非接触な分光光学的分析法がその候補としてあげられ、今、最も注目されている。一方で、これら分光学的手法により得られるスペクトルデータは、一般に分子内化学情報・分子間化学情報・物理学情報などの複雑で膨大な情報を含むことから、これらのデータを有効に活用するためには、スペクトルデータから目的情報を抽出する計量化学(chemometrics)11)的手法を適用することが不可欠である。特に、製薬部門では、NIRを用いた原料医薬品粉末や添加剤粉末の全量全品定性検査の実施が期待されてる。また、PATの実施例として製剤中の原料医薬品の添加物への薬物分布の検証として、混合処理中の主薬分散をNIRでモニタリングする試みが行われている。
医薬品結晶の非晶質化や結晶多形の調製は、難溶性薬物については溶解度が高まるため、製剤からの溶出性を増し、バイオアベイラビリティを改善する方法の一つとして利用されている。このような結晶形に関する原料医薬品の品質を評価する方法として、現状では、粉末X線回折(XRD)、熱量測定などにより、原料医薬品の抜き取り受け入れ検査が行われているが、様々な種類の化合物を全て安全確実に時間内に測定し、PATを実践することは、現状の方法では、不可能である。このため迅速検査法として非破壊・非接触なNIRケモメトリックス法による結晶化度や結晶多形含有量などの原料物性の検査が模索されている12)。
一方、医薬品は、一般に薬理活性を持つ原料粉末とその原料の特性を引き出すために加えられる賦形剤、崩壊剤、滑沢剤などの添加剤から構成される複合化剤であり、含有量が数パーセントの低含有量の場合も少なくない。これらの製剤中の原料医薬品の中に、結晶構造の違いによる多形現象を示す物が存在し、その結晶多形の物理化学的安定性が溶解性やバイオアベイラビリティに影響することがある。これらのことから混合粉末中でNIRケモメトリックス法による製剤中の原料医薬品粉末結晶多形含有量の評価に関する研究が行われている13)。
NIR法は、その操作が極めて簡便であり、試料を非破壊で測定できることから、NIRケモメトリックス法は、製剤の製造過程における迅速測定性からPATへの可能性が示唆される。このような背景から医薬品製造に関連する製剤設計分野で、計量化学は、最も注目される研究分野となっている。本編では、これらのPAT関連研究からさらに一歩進んだ製剤評価法として顆粒の流動性や錠剤硬度などの製剤特性そのものを非破壊測定法により評価することを試みた。
■NIR・ケモメトリックス法による顆粒特性の予測14)
高品質の医薬品を安定的に製造するためには医薬品製造過程における医薬品原料の物理化学的特性を十分に把握していくことが重要である。しかし、顆粒などの製剤は、原末医薬品のほかに賦形剤、結合剤、崩壊剤など複数の原料を混合することにより調製するために、出来あがった製剤の特性は、各原料粉末の結晶形、平均粒子径、粒度分布に影響を受ける。また、製剤特性は、調製時の造粒操作条件である装置容量、攪拌速度、温度などの影響も受ける。このため顆粒の製剤特性の理論的な予測が難しいことから、現在は、経験的な手法により製剤特性を制御している。そこで、これらの顆粒の製剤特性を科学的根拠に基づき制御することを目指して、製剤特性の解析とその予測を試みた。錠剤の製造行程の一部である打錠用顆粒調製法である攪拌造粒操作を取り上げた。練合水分量を変動させ調製した顆粒の製剤特性とNIRスペクトルの関係をケモメトリックス法により検討した。 NIRスペクトルの変動を主成分回帰分析法(PCR)を用いて解析し、調製した打錠原料顆粒の物理化学的特性を定量的に評価し、この原料顆粒から調製した錠剤の製剤特性を予測することを試みた。モデル薬物として解熱鎮痛剤であるアンチピリン0.5%、賦形剤として乳糖・デンプン、結合剤としてヒドロキシプロピルセルロースを混合した後、精製水(11~19%)を添加し、造粒、乾燥し、打錠用顆粒とした。続いて、打錠用顆粒にステアリン酸マグネシウム(以下MgSt)1%を添加し、応力試験機を用いて錠剤を調製した。これらの顆粒及び錠剤についてそれぞれメジアン径、安息角、圧縮度、錠剤硬度、空隙率、NIRを測定した。顆粒造粒時の練合水分量の増加に伴いメジアン径は増加し、粒子径の揃った顆粒が得られた。粒子径の大きさは添加する水分量による粒子同士の凝集、すなわち練合水分量の付着凝集力により顆粒粒子径が変動していることから、乾燥後の化学的組成は全て同一である。練合水分量によりメジアン径、顆粒流動性、圧縮率の異なる打錠用顆粒を原料として錠剤硬度、錠剤空隙率の異なる錠剤を調製した。このことから、顆粒の流動性や顆粒から調整される錠剤の成型特性の変動は、原料顆粒の粒子径や空隙率などの顆粒粒子の幾何学的な変化により、もたらされることがわかる。
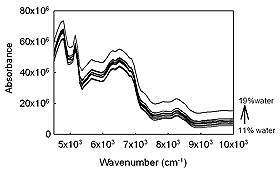
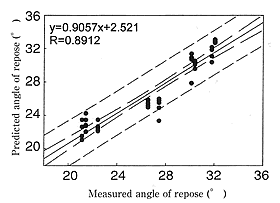
Fig.1に調製した顆粒剤のNIRスペクトルを示した。顆粒粒子径の変動は、NIRスペクトルのベースラインのシフトとして顕著に現れていることが示唆された。これらのNIRスペクトルからPCR法により解析したメジアン径の実測値と予測値の関係は、よい相関性を示し、NIRケモメトリックス法により製剤の複合処方の顆粒粒子径を測定できることが示された。これらのスペクトルから予測した顆粒の流動性の結果(Fig.2)はよい相関性を示した。このことから、原料顆粒の流動性は、NIR法により予測評価することができることがわかる。また、同様に成型後の錠剤空隙率や錠剤硬度に関しても予測が可能であることが示された。これらの製剤特性は、原料顆粒や錠剤の有効性を支配するパラメータであることから、顆粒の幾何学的変動によるスペクトル変化を基に評価された製剤特性の予測は、製剤の品質管理に有効であると思われる。同様に、原料顆粒のNIRスペクトルから粉末流動性や錠剤成型硬度などの製剤特性の予測を可能にしていることが理解される。
■NIRケモメトリックス法による滑沢剤混合過程が錠剤硬度に与える影響15)
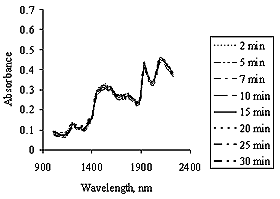
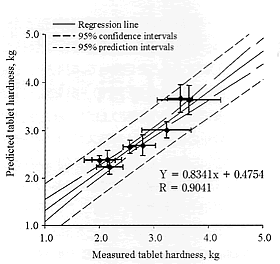
近年、機械技術の進歩と共に打錠の高速化と無人運転が進み、錠剤の大量生産が可能となっている。そしてこれらの高速打錠をするにあたり、MgStは打錠障害を防ぐ、必須の滑沢剤である。しかし、MgStは混合時間、混合方法等により、過混合により滑沢剤が粒子表面に疎水性皮膜を形成し、錠剤硬度の低下や溶解性の遅延をもたらすことが知られている。そこで、MgStの適正な混合時間を管理する目的で、錠剤の硬度変化を製錠することなく、混合粉末のNIR測定から粉末状態で錠剤硬度を予測することを目的として実験を行った。モデル薬物としてスルピリン10%、賦形剤として噴霧乾燥乳糖、コーンスターチをよく混合した後、滑沢剤としてMgStを1%添加し、V型混合機で混合したものを経時的に採取し、NIRを測定した。これらのNIRの混合による変化をFig.3に示した。また各試料を打錠機で圧縮して錠剤を調製し、錠剤硬度を測定した。NIRデータに基づきPCR法を用いて解析し、実測値と予測値との相関を調べた。MgSt混合時間による錠剤引張り強度が変化し、MgStの混合時間が増加するにしたがい、錠剤引張り強度が低下することが確認された。Fig.4にNIRスペクトルからPCRにより解析した錠剤引張り強度の実測値と予測値の関係を示した。ここに示したように回帰式 Y= 0.8341x + 0.4754、R = 0.9041で表され実測値と予測値の間に良好な相関が得られた。
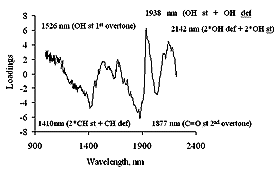
Fig.5にこれらの検量モデルのRegression vectorを示した。この相関式の重みを表すRegression vectorにおいて、正の相関にでているピーク1526nmは、(OH st 1stovertone)、1938nmは、(OH st + OH def H20)、2142nmは、(2*OH def + 2*OH st)に関連する吸収であり、これらの官能基は、賦形剤に起因する。反対に負の相関にでているピーク1410nm(2*CH st + CH def)と1877nm(C=O st 2ndovertone)は滑沢剤に起因した。これらのことから賦形剤に関連する官能基と滑沢剤に起因する官能基は、錠剤硬度に対して反対の方向に作用していることが示される。錠剤の硬度が、賦形剤の粒子間の水素結合に依存すると考えるとき、混合過程における滑沢剤の賦形剤粒子表面への分布・展延作用が錠剤硬度に影響を与えていることが示唆される。
■結言
製剤の物理化学的特性には様々な因子が関与しているが、その個々の因子と物理化学的特性を科学的に解明することで製剤の物理化学的特性を制御することが可能である。中でも練合水分量⇔粒子径⇔物理化学的特性の間には大きな相関性があり、練合水分量を調節し顆粒の粒子径と顆粒内内部構造を制御することが可能である。また、製剤特性に大きな影響を与える滑沢剤の混合過程において、滑沢剤の処方中の分布と賦形剤との相互作用をNIRにより測定することができる。このことにより、原料混合粉末のNIRスペクトルから錠剤圧縮後の錠剤硬度を予測できることがわかる。製剤原料の状態を表すNIRスペクトルから得られる物理化学的情報を統計学的に解析することで、その最終生産製剤の製剤学的特性までも制御し、予測することがファーマコインフォマティクス研究として可能であることが示された。
参考文献